Nyeri adalah sensasi tidak
menyenangkan lokal pada
suatu bagian tubuh. Ini sering digambarkan dalam hal proses penetrasi atau
jaringan-destruktif (misalnya,
tertusuk, terbakar, terputar, robek, teremas)
dan / atau
dari tubuh atau reaksi emosional (misalnya, takut, memuakkan).
Selanjutnya, setiap nyeri intensitas sedang atau tinggi
disertai oleh kecemasan dan dorongan untuk melarikan diri atau mengakhiri perasaan tersebut. Hal ini menggambarkan dualitas nyeri: baik sensasi
maupun emosi. Dikatakan akut ketika timbul nyeri khas berhubungan dengan gairah perilaku dan respon stres
yang terdiri dari peningkatan tekanan darah, denyut jantung,
diameter pupil, dan
kadar kortisol plasma. Selain itu, otot lokal
berkontraksi (misalnya, fleksi
tungkai, perut dinding
kekakuan) sering ditemukan.
MEKANISME PERIPHERAL
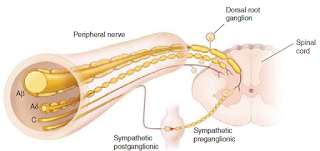
Aferen nociceptor primer Sebuah saraf perifer terdiri dari akson
dari tiga jenis neuron: aferen sensorik primer, motor neuron, dan simpatik neuron
postganglionik. Badan sel aferen sensorik primer terletak di ganglia akar
dorsal dalam foramen vertebralis. Akson aferen primer memiliki dua cabang: salah
satu untuk proyeksi pusat ke tulang belakang dan proyeksi perifer lainnya untuk
menginervasi jaringan. Aferen primer diklasifikasikan oleh diameter mereka,
derajat mielinisasi, dan kecepatan konduksi.
Gambar: Komponen
saraf perifer
Diameter terbesar serat aferen, A-beta (Aβ), merespon secara maksimal terhadap sentuhan ringan dan/atau rangsangan bergerak; yang terdapat terutama di saraf yang menginervasi kulit. Pada individu normal, aktivitas serat ini tidak menghasilkan rasa sakit. Ada dua kelas lainnya serat saraf aferen primer: A-delta (Aδ) berdiameter mielin kecil dan akson yang tidak bermielin (C). Serat ini terdapat dalam saraf di struktur kulit, somatik bagian dalam dan viseral. Beberapa jaringan, seperti kornea, dipersarafi hanya dengan serat aferen Aδ dan C. Kebanyakan Aδ dan C aferen serat merespon secara maksimal hanya untuk rangsangan intens (menyakitkan) dan menghasilkan pengalaman sakit subjektif ketika mereka dirangsang; ini mendefinisikan mereka sebagai aferen nociceptors primer (reseptor nyeri). Kemampuan untuk mendeteksi rangsangan yang menyakitkan benar-benar dihapuskan ketika konduksi di akson serat Aδ dan C diblokir.
Setiap aferen nociceptors primer
dapat menanggapi beberapa berbagai jenis rangsangan berbahaya. Sebagai contoh,
sebagian besar nociceptors menanggapi panas; dingin yang intens; distorsi
mekanik yang intens, seperti cubitan; perubahan pH, khususnya lingkungan asam;
dan iritasi kimia termasuk adenosine triphosphate (ATP), serotonin, bradikinin,
dan histamin.
Sensitisasi
Ketika rangsangan intens,
berulang, atau berkepanjangan diterapkan untuk jaringan yang rusak atau
meradang, ambang batas untuk mengaktifkan aferen nociceptors primer diturunkan,
dan frekuensi penembakan yang lebih tinggi untuk semua intensitas stimulus.
Mediator inflamasi seperti bradikinin, faktor pertumbuhan-saraf, beberapa
prostaglandin, dan leukotrien berkontribusi untuk proses ini, yang disebut
sensitisasi. Sensitisasi terjadi di tingkat saraf perifer terminal (sensitisasi
perifer) serta sebagai pada tingkat dorsal horn sumsum tulang belakang
(sensitisasi sentral). Sensitisasi perifer terjadi pada jaringan yang rusak
atau meradang, ketika mediator inflamasi mengaktifkan sinyal transduksi
intraseluler di nociceptors, mendorong peningkatan produksi, transportasi, dan
membran penyisipan saluran ion kimia-gated dan tegangan-gated. Perubahan ini
meningkatkan rangsangan dari nociceptor terminal dan menurunkan ambang batas
mereka untuk aktivasi oleh mekanik, termal, dan rangsangan kimia. Sensitisasi
sentral terjadi ketika aktivitas, dihasilkan oleh nociceptors selama inflamasi,
meningkatkan rangsangan yang dari sel-sel saraf di dorsal horn sumsum tulang
belakang. Cedera berikut dan sensitisasi dihasilkan, biasanya rangsangan
berbahaya dapat menghasilkan nyeri (disebut allodynia). Sensitisasi adalah
proses yang penting secara klinis yang memberikan kontribusi untuk rasa sakit
dan hiperalgesia (intensitas nyeri meningkat dalam menanggapi stimulus berbahaya
yang sama). Sebuah contoh yang mencolok dari sensitisasi adalah kulit terbakar
matahari, di mana sakit parah dapat diproduksi oleh tamparan lembut di bagian
belakang atau mandi hangat. Sensitisasi sangat penting terutama untuk nyeri dan
nyeri tekan di dalam jaringan. Organ viesral biasanya relatif tidak sensitif
terhadap rangsangan mekanik dan termal ysng berbahaya, meskipun organ viseral
yang berongga menghasilkan ketidaknyamanan yang signifikan ketika sangat penuh.
Sebaliknya, bila dipengaruhi oleh proses penyakit dengan komponen inflamasi,
struktur-struktur dalam seperti sendi atau organ viseral yang berongga khas
menjadi sensitif terhadap stimulasi mekanik.
Sebagian besar serat aferen Aδ dan C menginervasi organ viseral benar-benar tidak sensitif pada jaringan yang normal. Artinya, mereka tidak dapat diaktifkan dengan rangsangan mekanik yang diketahui atau termal dan tidak aktif secara spontan. Namun, dengan adanya mediator inflamasi, aferen ini menjadi sensitif terhadap rangsangan mekanik. Aferen seperti telah disebut nosiseptor diam, dan sifat karakteristik mereka dapat menjelaskan bagaimana, di bawah patologis kondisi, struktur yang relatif tidak sensitif dalam dapat menjadi sumber rasa sakit yang parah dan melemahkan. PH rendah, prostaglandin, leukotrien, dan mediator inflamasi lainnya seperti
bradikinin memainkan peran penting dalam sensitisasi.
Sebagian besar serat aferen Aδ dan C menginervasi organ viseral benar-benar tidak sensitif pada jaringan yang normal. Artinya, mereka tidak dapat diaktifkan dengan rangsangan mekanik yang diketahui atau termal dan tidak aktif secara spontan. Namun, dengan adanya mediator inflamasi, aferen ini menjadi sensitif terhadap rangsangan mekanik. Aferen seperti telah disebut nosiseptor diam, dan sifat karakteristik mereka dapat menjelaskan bagaimana, di bawah patologis kondisi, struktur yang relatif tidak sensitif dalam dapat menjadi sumber rasa sakit yang parah dan melemahkan. PH rendah, prostaglandin, leukotrien, dan mediator inflamasi lainnya seperti
bradikinin memainkan peran penting dalam sensitisasi.
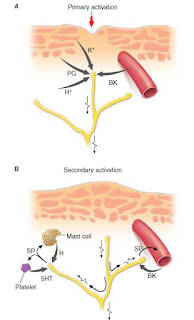
Peradangan Nociceptor-Induced Aferen nociceptors primer juga memiliki fungsi neuroefektor. Kebanyakan nociceptors mengandung mediator polipeptida yang dilepaskan dari terminal perifer mereka ketika mereka diaktifkan. Contohnya adalah substansi P, 11-asam amino peptida. Zat P dilepaskan dari nosiseptor aferen primer dan memiliki beberapa kegiatan biologis yaitu vasodilator kuat, degranulasi sel mast, adalah chemoattractant untuk leukosit, dan meningkatkan produksi
dan melepaskan mediator inflamasi. Menariknya, eksperimen penipisan dari substansi P dari sendi mengurangi keparahan arthritis. Aferen nociceptors primer adalah tidak hanya agen yang pasif
terhadap ancaman cedera jaringan, tetapi juga berperan aktif dalam perlindungan jaringan melalui fungsi neuroefektor ini.
Gambar: Aktivasi, sensitisasi,
dan penyebaran sensitisasi aferen
nociceptors primer
MEKANISME SENTRAL
Sumsum tulang belakang dan Referred Pain (Nyeri Alih) Akson aferen nociceptors primer
masuk sumsum tulang belakang melalui akar dorsal. Mereka berhenti dalam dorsal horn dari gray mater tulang belakang. Terminal akson aferen primer menghubungi neuron spinal yang mengirimkan sinyal rasa sakit ke situs otak yang terlibat dalam persepsi nyeri. Ketika aferen utama diaktifkan oleh rangsangan berbahaya, mereka melepaskan neurotransmitter dari terminal mereka yang merangsang neuron sumsum tulang belakang. Neurotransmitter utama dikeluarkan yaitu glutamat, yang dengan cepat “menggairahkan” neuron dorsal horn. Terminal aferen nociceptor utama juga mengeluarkan peptida, termasuk substansi P dan kalsitonin terkait peptida-gen, yang menghasilkan eksitasi lebih lambat dan lebih tahan lama dari neuron dorsal horn. Setiap akson aferen primer melakukan kontak dengan banyak neuron di tulang belakang, dan masing-masing neuron spinal menerima input konvergen dari banyak aferen primer.
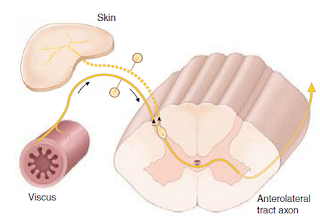
Konvergensi input sensorik menjadi transmisi nyeri tunggal pada neuron tulang belakang sangat penting karena mendasari fenomena dari referred pain (nyeri alih) . Semua neuron spinal yang menerima input dari struktur muskuloskeletal bagian dalam dan viseral juga menerima input
dari kulit. Pola konvergensi ditentukan oleh segmen tulang belakang dari akar dorsal ganglion yang memasok persarafan aferen dari struktur. Misalnya, aferen yang memasok pusat diafragma yang berasal dari akar dorsal ganglia serviks ketiga dan keempat. Aferen primer dengan badan sel yang dipasok oleh ganglia yang sama dari kulit bahu dan leher bagian bawah. Dengan demikian, input sensorik dari baik kulit bahu maupun diafragma sentral berkumpul di neuron transmisi nyeri di segmen tulang belakang serviks ketiga dan keempat. Karena konvergensi ini dan fakta bahwa neuron tulang belakang yang paling sering diaktifkan oleh input dari kulit, aktivitas menstimulasi neuron di tulang belakang dengan input dari struktur-struktur dalam yang disalahartikan oleh pasien ke tempat yang kira-kira sesuai dengan daerah kulit dipersarafi oleh segmen tulang belakang yang sama. Dengan demikian, peradangan dekat diafragma pusat sering dilaporkan sebagai ketidaknyamanan pada bahu. Perpindahan sensasi nyeri dari tempat cedera yang sebenarnya dikenal sebagai reffered pain (nyeri alih).
Sumsum tulang belakang dan Referred Pain (Nyeri Alih) Akson aferen nociceptors primer
masuk sumsum tulang belakang melalui akar dorsal. Mereka berhenti dalam dorsal horn dari gray mater tulang belakang. Terminal akson aferen primer menghubungi neuron spinal yang mengirimkan sinyal rasa sakit ke situs otak yang terlibat dalam persepsi nyeri. Ketika aferen utama diaktifkan oleh rangsangan berbahaya, mereka melepaskan neurotransmitter dari terminal mereka yang merangsang neuron sumsum tulang belakang. Neurotransmitter utama dikeluarkan yaitu glutamat, yang dengan cepat “menggairahkan” neuron dorsal horn. Terminal aferen nociceptor utama juga mengeluarkan peptida, termasuk substansi P dan kalsitonin terkait peptida-gen, yang menghasilkan eksitasi lebih lambat dan lebih tahan lama dari neuron dorsal horn. Setiap akson aferen primer melakukan kontak dengan banyak neuron di tulang belakang, dan masing-masing neuron spinal menerima input konvergen dari banyak aferen primer.
Konvergensi input sensorik menjadi transmisi nyeri tunggal pada neuron tulang belakang sangat penting karena mendasari fenomena dari referred pain (nyeri alih) . Semua neuron spinal yang menerima input dari struktur muskuloskeletal bagian dalam dan viseral juga menerima input
dari kulit. Pola konvergensi ditentukan oleh segmen tulang belakang dari akar dorsal ganglion yang memasok persarafan aferen dari struktur. Misalnya, aferen yang memasok pusat diafragma yang berasal dari akar dorsal ganglia serviks ketiga dan keempat. Aferen primer dengan badan sel yang dipasok oleh ganglia yang sama dari kulit bahu dan leher bagian bawah. Dengan demikian, input sensorik dari baik kulit bahu maupun diafragma sentral berkumpul di neuron transmisi nyeri di segmen tulang belakang serviks ketiga dan keempat. Karena konvergensi ini dan fakta bahwa neuron tulang belakang yang paling sering diaktifkan oleh input dari kulit, aktivitas menstimulasi neuron di tulang belakang dengan input dari struktur-struktur dalam yang disalahartikan oleh pasien ke tempat yang kira-kira sesuai dengan daerah kulit dipersarafi oleh segmen tulang belakang yang sama. Dengan demikian, peradangan dekat diafragma pusat sering dilaporkan sebagai ketidaknyamanan pada bahu. Perpindahan sensasi nyeri dari tempat cedera yang sebenarnya dikenal sebagai reffered pain (nyeri alih).
Gambar: Nyeri Alih
(Reffered Pain)
Jalur
Naik (Ascending Pathway) Mayoritas neuron spinal
dihubungi oleh aferen nociceptors
primer mengirim akson
mereka ke kontralateral thalamus.
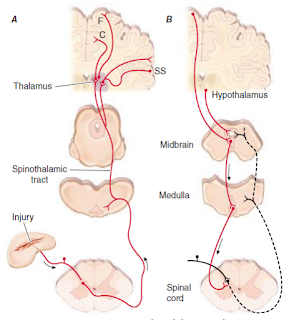
Akson ini membentuk traktus spinotalamikus kontralateral, yang terletak di white mater anterolateral dari sumsum
tulang belakang, lateral
tepi medula, dan pons lateral dan otak tengah. Jalur spinotalamikus penting untuk sensasi nyeri pada manusia. Gangguan dari jalur ini menghasilkan defisit permanen untuk menilai nyeri dan suhu.
Akson traktus spinotalamikus naik ke beberapa daerah thalamus.
Ada perbedaan yang sangat besar dari sinyal nyeri dari thalamic ini ke beberapa daerah yang berbeda di korteks serebral yang mengacu pada aspek berbeda dari pengalaman nyeri. Salah satu proyeksi thalamic adalah untuk korteks somatosensori. Proyeksi ini menengahi aspek murni sensorik nyeri, yaitu, lokasi, intensitas, dan kualitas. Proyek neuron thalamic lain untuk daerah korteks yang terkait dengan respon emosional, seperti gyrus cingulate dan daerah lain di lobus frontal, termasuk korteks insular. Jalur korteks frontal ini mengacu pada dimensi nyeri yang emosional afektif atau tidak menyenangkan. Di dimensi afektif ini, nyeri menghasilkan penderitaan dan diberikannya kontrol yang ampuh terhadap perilaku individu. Karena dimensi ini, rasa takut adalah pendamping sakit. Sebagai konsekuensi, cedera atau lesi pembedahan pada daerah korteks frontal yang aktif oleh rangsangan yang menyakitkan bisa mengurangi dampak emosional dari rasa sakit dan sebagian besar menyisakan kemampuan individu untuk mengenali rangsangan berbahaya yang menyakitkan.
tepi medula, dan pons lateral dan otak tengah. Jalur spinotalamikus penting untuk sensasi nyeri pada manusia. Gangguan dari jalur ini menghasilkan defisit permanen untuk menilai nyeri dan suhu.
Akson traktus spinotalamikus naik ke beberapa daerah thalamus.
Ada perbedaan yang sangat besar dari sinyal nyeri dari thalamic ini ke beberapa daerah yang berbeda di korteks serebral yang mengacu pada aspek berbeda dari pengalaman nyeri. Salah satu proyeksi thalamic adalah untuk korteks somatosensori. Proyeksi ini menengahi aspek murni sensorik nyeri, yaitu, lokasi, intensitas, dan kualitas. Proyek neuron thalamic lain untuk daerah korteks yang terkait dengan respon emosional, seperti gyrus cingulate dan daerah lain di lobus frontal, termasuk korteks insular. Jalur korteks frontal ini mengacu pada dimensi nyeri yang emosional afektif atau tidak menyenangkan. Di dimensi afektif ini, nyeri menghasilkan penderitaan dan diberikannya kontrol yang ampuh terhadap perilaku individu. Karena dimensi ini, rasa takut adalah pendamping sakit. Sebagai konsekuensi, cedera atau lesi pembedahan pada daerah korteks frontal yang aktif oleh rangsangan yang menyakitkan bisa mengurangi dampak emosional dari rasa sakit dan sebagian besar menyisakan kemampuan individu untuk mengenali rangsangan berbahaya yang menyakitkan.
Gambar: (A) Ascending
Pathways (B) Modulasi Nyeri
MODULASI NYERI
Rasa sakit
yang dihasilkan oleh cedera akan
sangat variabel dalam situasi yang
berbeda dan pada individu yang berbeda pula. Sebagai contoh, atlet
telah dikenal dapat menahan patah tulang
yang serius dengan hanya sedikit nyeri,
dan survei Beecher
pada Perang Dunia II mengungkapkan
bahwa banyak tentara dalam pertempuran yang tidak terganggu oleh
kesakitan yang akan dihasilkan
pada cedera pasien sipil. Selanjutnya, bahkan adanya sugesti bahwa pengobatan akan mengurangi rasa sakit dapat memiliki efek analgesik signifikan (efek plasebo). Di sisi lain, banyak pasien menemukan bahkan luka kecil (seperti venipuncture) menakutkan dan tak tertahankan, dan
harapan nyeri dapat menyebabkan rasa sakit bahkan tanpa stimulus yang berbahaya.
Sugesti bahwa adanya rasa sakit akan memperburuk administrasi berikut dari zat inert dapat meningkatkan intensitas dirasakan nya (efek nocebo).
pada cedera pasien sipil. Selanjutnya, bahkan adanya sugesti bahwa pengobatan akan mengurangi rasa sakit dapat memiliki efek analgesik signifikan (efek plasebo). Di sisi lain, banyak pasien menemukan bahkan luka kecil (seperti venipuncture) menakutkan dan tak tertahankan, dan
harapan nyeri dapat menyebabkan rasa sakit bahkan tanpa stimulus yang berbahaya.
Sugesti bahwa adanya rasa sakit akan memperburuk administrasi berikut dari zat inert dapat meningkatkan intensitas dirasakan nya (efek nocebo).
Pengaruh kuat dari ekspektasi
dan variabel psikologis lainnya pada intensitas nyeri yang dirasakan
diperantarai oleh sirkuit otak yang memodulasi aktivitas jalur transmisi nyeri. Satu dari sirkuit ini
memiliki link ke hipotalamus,
otak tengah, dan medula,
dan selektif mengendalikan
neuron transmisi nyeri di tulang belakang melalui jalur menurun (descending pathways).
Studi pencitraan
otak manusia telah mengimplikasikan sirkuit modulasi nyeri ini dalam efek penghilang rasa sakit dari perhatian, sugesti,
dan obat analgesik opioid. Selanjutnya, masing-masing
struktur komponen jalur mengandung reseptor opioid dan sensitif terhadap aplikasi langsung dari obat opioid. Pada hewan, lesi dari sistem modulatory menurun dapat mengurangi efek analgesik opioid sistemik seperti morfin. Seiring dengan reseptor opioid, inti komponen sirkuit modulasi nyeri ini mengandung peptida opioid endogen seperti enkephalins dan β-endorphin.
struktur komponen jalur mengandung reseptor opioid dan sensitif terhadap aplikasi langsung dari obat opioid. Pada hewan, lesi dari sistem modulatory menurun dapat mengurangi efek analgesik opioid sistemik seperti morfin. Seiring dengan reseptor opioid, inti komponen sirkuit modulasi nyeri ini mengandung peptida opioid endogen seperti enkephalins dan β-endorphin.
Cara yang paling
dapat diandalkan untuk mengaktifkan
sistem modulasi endogen
dimediasi-opioid ini adalah dengan sugesti
dari nyeri atau
dengan emosi yang kuat yang diarahkan jauh dari rasa sakit (misalnya, selama ancaman berat atau kompetisi atletik). Bahkan, penghilang rasa sakit opioid endogen dilepaskan mengikuti prosedur bedah dan pada pasien yang
diberikan plasebo untuk menghilangkan rasa sakit.
Sirkuit modulasi-salit
dapat meningkatkan serta menekan nyeri. Kedua neuron penghambat nyeri dan neuron
yang memfasilitasi dalam proyeksi medula
dan mengontrol neuron transmisi nyeri pada tulang belakang. Karena neuron transmisi nyeri dapat diaktifkan dengan neuron modulatory, secara teoritis mungkin dapat dihasilkan sinyal rasa sakit tanpa stimulus
berbahaya di perifer. Bahkan,
studi pencitraan fungsional manusia telah menunjukkan bahwa peningkatan
aktivitas di sirkuit ini selama sakit kepala migrain. Sebuah rangkaian sentral yang memfasilitasi rasa sakit dapat menjelaskan temuan bahwa nyeri dapat disebabkan oleh sugesti
atau ditingkatkan dengan harapan
dan menyediakan gambaran untuk memahami faktor-faktor psikologis tentang bagaimana penerapannya untuk nyeri kronis.
Sumber: Harrison Internal Medicine edisi 9 hal 173-175
Sumber: Harrison Internal Medicine edisi 9 hal 173-175

0 Response to "Nyeri: Mekanisme, Transmisi, dan Modulasi"
Post a Comment